Il Dr Lavezzari ha cominciato ad utilizzare le cellule staminali dal 2010 ed ha studiato il loro impiego nel trapianto di capelli in collaborazione con un Istituto di Ricerche svizzero.
Alcuni studi,come “Adipociti immaturi e fattori bio-attivi, nuovi induttori dell’hair cycling” sono stati presentati in congressi internazionali.
L'INTERVENTO E LE SUE FASI
per saperne di più:
ADIPOCITI IMMATURI E FATTORI BIO-ATTIVI NUOVI INDUTTORI DELL’HAIR CYCLING

Le nicchie staminali, zone tissutali in cui c’è un’alta concentrazione di cellule staminali pluripotenti, sono essenziali per il rinnovamento e il mantenimento di qualsiasi tessuto corporeo.
In particolare, la nicchia di cellule staminali del follicolo che si trova nel Bulge promuove il rinnovamento e la rigenerazione del capello durante le diverse fasi dell’Hair Cycle.
Per dare il via alla fase Anagen, le cellule del Bulge migrano verso la papilla dermica, dove si differenziano e permettono la crescita del capello.
Innumerevoli sono i fattori che promuovono l’attività delle cellule staminali del follicolo. Tra questi riconosciamo: le molecole segnale rilasciate dalla papilla dermica e segnali estrinseci quali Bone Morphogenetic Proteins (BMPs), Fibroblast Growth Factor (FGFs) e Platelet Derived Growth Factors (PDGFs).
Uno studio recente, pubblicato sulla rivista scientifica Cell (Festa et al., Adipocite lineage cell contribute to skin stem cell niche to drive hair cycling, Cell 146: 761-771, 2 sept 2011) ha dimostrato che anche gli adipociti immaturi intradermici hanno un ruolo fondamentale nell’induzione dell’attività delle cellule staminali del Bulge.
Durante il ciclo di vitale del follicolo il tessuto adiposo intradermico incrementa le sue dimensioni sia a causa dell’attivazione di precursori adipocitici immaturi, sia grazie alla sintesi de novo di cellule adipose. La proliferazione di tali cellule è stimolata nel corso la fase Telogen e all’inizio della fase Anagen.
In pre-clinica si è osservato che topi privi di adipociti immaturi a livello del follicolo, non sono in grado di iniziare la fase Anagen rimanendo così bloccati in Telogen statica, mentre topi che presentano pre-adipociti ma non sono in grado di indurne la maturazione, vanno in contro a un normale ciclo di crescita del capello. I dati ottenuti con modelli in vivo confermano i risultati ottenuti in vitro avvalorando la tesi secondo cui non sono gli adipociti maturi a fungere da attivatori per le cellule staminali del Bulge, bensì sono gli adipociti immaturi a svolgere questo ruolo fondamentale; senza tali cellule, infatti, il capello non riesce a continuare il suo ciclo di crescita e rimane bloccato nella fase Telogen, Figura 1.
Dagli studi da noi condotti, con la collaborazione del Cardiocentro di Lugano, è emerso un interessantissimo dato che correla con quanto recentemente scoperto in pre-clinica.
La sospensione cellulare che viene iniettata al termine di interventi di autotrapianto consiste di un pool eterogeneo di cellule costituito da: eritrociti, cellule epiteliali, 5% di cellule staminali adipose (ASC) e un 90% di cellule vive che corrispondono ad adipociti immaturi, ossia cellule staminali adipose al primo stadio di differenziamento, Figura 2, 3.
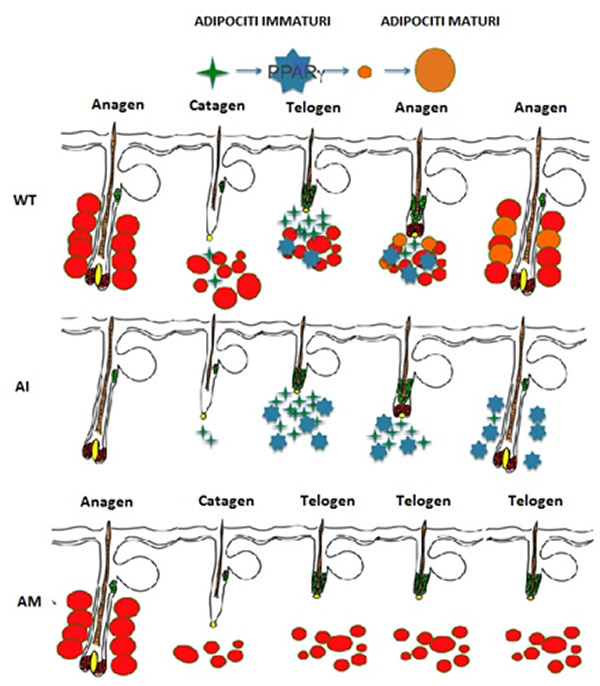
Figura 1. Modello del ruolo degli Adipociti nell'Hair Cycle di topi Wild Type (WT) o con difetti nell'adipogenesi.
La proliferazione del lineage adipocitico è stimolata durante la fase di regressione del follicolo (Catagen) in modo da incrementare il numero di precursori adipocitici durante la fase Telogen e Anagen, WT. Topi AI, che mancano di adipociti maturi ma presentano pre-adipociti, rigenerano il follicolo come i WT; topi AM che mancano di adipociti immaturi rimangono in fase Telogen senza dare il via a un nuovo ciclo di crescita del capello.

Figura 2. Visualizzazione al microscopio della sospensione cellulare iniettata nella zona soggetta ad autotrapianto.
Le cellule vive sono ben visibili perché internalizzano un colorante vitale che si lega al DNA e le rende fluorescenti, di contro le cellule morte risultano nere; gli eritrociti sono invece cellule anucleate più piccole delle normali cellule. I detriti cellulari e tissutali sono presenti per via della metodica di frammentazione meccanica del tessuto adiposo.
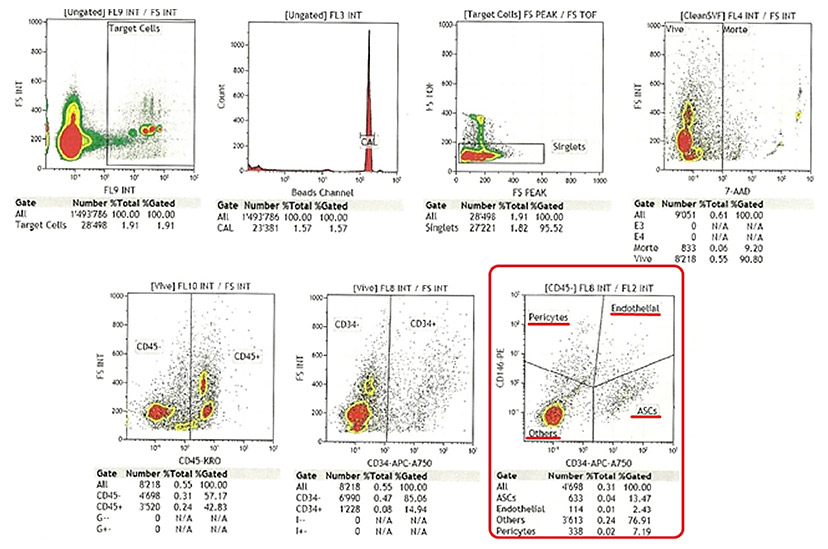
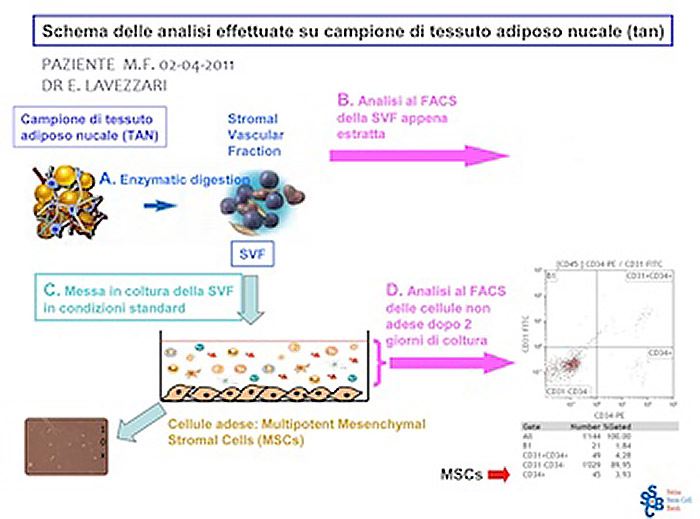
Figura 3. Analisi FACS della composizione cellulare del Pool di cellule iniettato a seguito di autotrapianto.
L’analisi mostra chiaramente la presenza di ASC (Adipose Stem Cell), Periciti,cellule endoteliali, Eritrociti e Others, riconducibili ad adipociti immaturi.
Considerato ciò che è emerso dagli studi di Festa et al., che dimostrano chiaramente come sia necessaria la presenza di adipociti immaturi per indurre il follicolo a dare il via alla fase Anagen di crescita del capello, iniettando questa sospensione cellulare a livello della zona soggetta all’autotrapianto si va ad arricchire il naturale back ground cellulare del tessuto, aumentando il numero di cellule del lineage adipocitico e inducendo un effetto positivo sulle cellule staminali del follicolo. Tali cellule entrano così in mitogenesi favorendo la crescita del capello.

Sono quindi gli adipociti immaturi e non solo le staminali adipose progenitrici a esercitare effetti positivi sui capelli trapiantati, prolungandone la fase Anagen e stimolandone il mantenimento.
Bisogna considerare inoltre che la sospensione cellulare iniettata al termine dell’autotrapianto viene preparata utilizzando un processo di omogeneizzazione del tessuto adiposo nucale basato su frammentazione meccanica. Tale processo è abbastanza aggressivo sui tessuti e,oltre a permettere di separare le cellule, promuove la rottura degli adipociti maturi, cellule vacuolate molto fragili. Gli adipociti maturi sono naturalmente ricchi di fattori bio-attivi i quali, una volta liberati ed iniettati nella zona soggetta all’autotrapianto, agiscono a livello paracrino favorendo la crescita e l’attecchimento dei capelli trapiantati.
In conclusione, la sospensione cellulare iniettata oltre a contenere un discreto quantitativo di cellule staminali mesenchimali, è ricca di adipociti immaturi e fattori bio-attivi che favoriscono entrambi la mitogenesi delle cellule del Bulge e quindi la crescita e il mantenimento dei capelli trapiantati.
Dr. Emilio Lavezzari
- 335-6129428
- 0041-79-4710331
- lavezzari@bluewin.ch
- www.capelli.info